科学界对癌症疗法的探索从未停歇,尤其聚焦于那些通过触发细胞凋亡来消灭癌细胞的治疗手段。细胞凋亡,又称程序性细胞死亡,是一种生物体内自然发生的有序过程,其目的在于移除受损或过时的细胞。而一些癌细胞通过各种机会主义手段,成功规避了治疗所诱发的凋亡,从而引致了治疗耐药性和癌症的重新发作。因此,如何规避掉那些能够逃逸现有治疗的癌细胞,成为了新的课题。

2023年2月6日,来自德克萨斯大学MD安德森癌症中心的甘波谊和陈俊杰教授团队在Nature Cell Biology杂志发表了题为“Actin cytoskeleton vulnerability to disulfide stress mediates disulfidptosis”的研究。该研究详细介绍了一种以前无法解释的细胞死亡类型——Disulfidptosis(二硫死亡或双硫死亡),可能为新的癌症治疗策略打开大门。
该研究表明,当SLC7A11蛋白高表达的细胞遭受葡萄糖饥饿时,就会触发双硫死亡。在临床前模型中,用葡萄糖抑制剂治疗可诱导SLC7A11高表达的癌细胞双硫化,有效抑制肿瘤生长,且对正常组织无明显毒性。
1研究背景
癌细胞为了适应恶劣的微环境,如营养缺乏,可能会激活一些独特的细胞死亡途径。过去的研究已经识别了多种细胞死亡形式,如凋亡、坏死、自噬性细胞死亡和铁死亡等。而在SLC7A11高表达的癌细胞中,在葡萄糖饥饿条件下,会发生一种尚未明确的细胞死亡形式,本研究的目标是探讨这种细胞死亡的机制。
2研究发现
在SLC7A11高表达细胞中,葡萄糖饥饿导致内部硫化物(如半胱氨酸)异常积累,引发硫化物应激,导致细胞骨架蛋白间形成异常二硫键和肌动蛋白(F-actin)崩溃,这是一种与已知凋亡和铁死亡不同的细胞死亡形式,被命名为“硫键相关细胞死亡”(disulfidptosis)。
3临床意义
在某些类型的癌细胞中,SLC7A11的异常高表达与癌细胞的生长和存活密切相关。同时,这些细胞在葡萄糖饥饿状态下对硫化物应激更为敏感,导致硫键相关细胞死亡。因此,通过引导这种特定的细胞死亡,或通过靶向SLC7A11进行动态调节,可能成为一种新的抗癌治疗策略。
4实验策略
使用化学蛋白质组学分析,确定了在SLC7A11高表达细胞中,葡萄糖饥饿状态下硫化应激导致的蛋白质间二硫键的形成。CRISPR基因编辑技术用于证明WAVE调节复合体(促进肌动蛋白聚合和假足形成的关键部分)的失活能够抑制硫键相关细胞死亡,而Rac1的持续激活促进了这种细胞死亡。在动物模型中证明了SLC7A11高表达的肿瘤细胞对葡萄糖转运抑制剂尤其敏感,这些抑制剂可以通过诱导硫键相关细胞死亡来抑制肿瘤生长。
5数据解读
图 1: 葡萄糖匮乏环境下SLC7A11高表达细胞中的独特细胞死亡形式
研究确定了SLC7A11高表达细胞在葡萄糖饥饿条件下经历了一种与已知细胞死亡形式不同的死亡过程(disulfidptosis)。
细胞用多种细胞死亡抑制剂(包括Ferrostatin-1, Deferoxamine, Z-VAD等)进行干预,发现这些抑制剂无法阻止细胞死亡。
进一步验证发现,SLC7A11的缺失可阻止细胞在无糖培养条件下死亡。
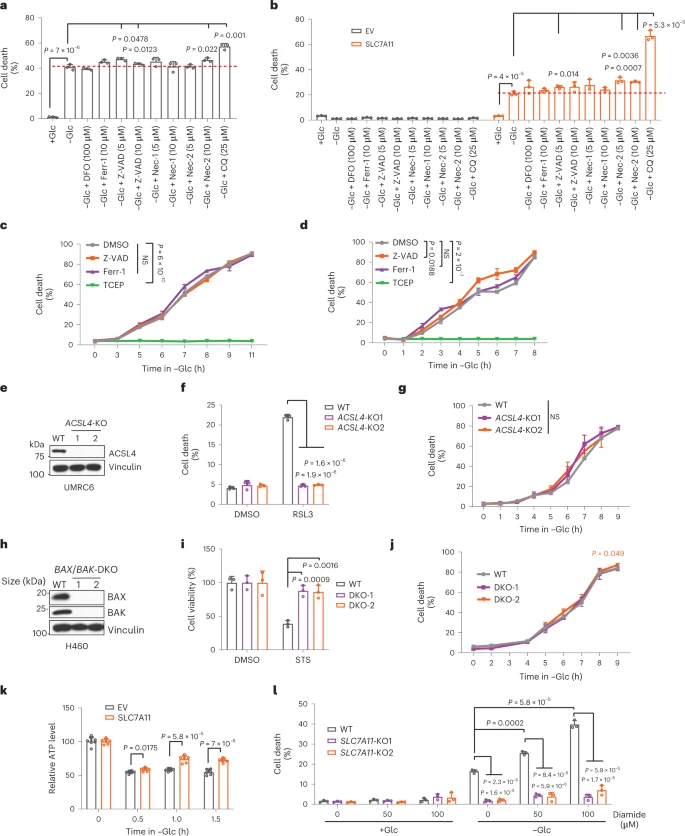
图 2: 葡萄糖饥饿状态下SLC7A11高表达细胞的蛋白质组分析
通过化学蛋白组学确定了糖酵解受损后增多的含二硫键的肽段。
基因本体(GO)富集分析表明这些蛋白质主要涉及细胞骨架和细胞黏附过程。
分析揭示了多个蛋白中二硫键数量的增加,特别是在肌动蛋白相关蛋白中。
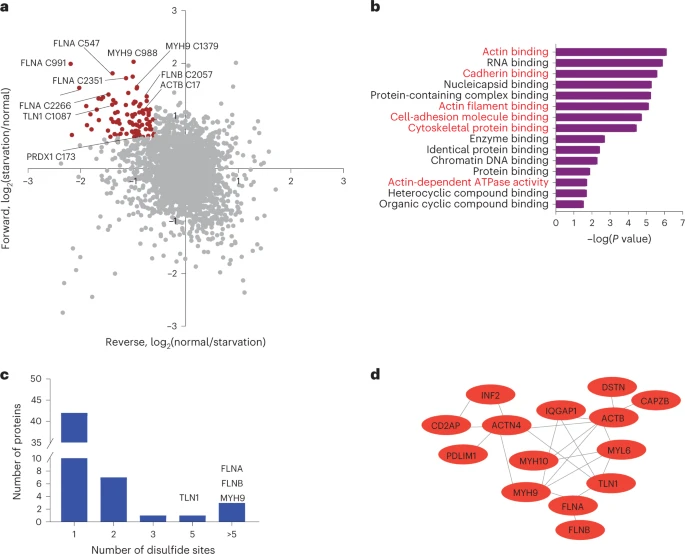
图 3: disulfidptosis中的细胞骨架蛋白二硫键
实验显示在无糖条件下细胞骨架蛋白表现出迁移减慢现象,而这种改变在SLC7A11基因敲除细胞中并未观察到。
增加的NADP+/NADPH比率表明二硫键的形成可能是由细胞内NADPH的耗尽导致的。
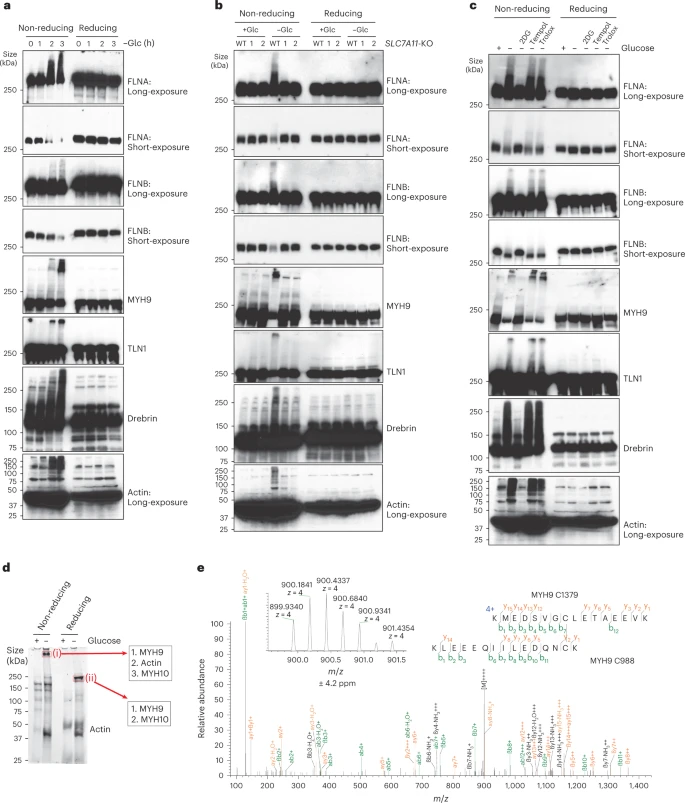
图 4: disulfidptosis期间F-actin的收缩
葡萄糖饥饿状态下细胞中F-actin出现了明显的收缩和膜脱离现象。
误点修复失败的细胞可能会导致细胞骨架组织的崩溃和随后的细胞死亡。
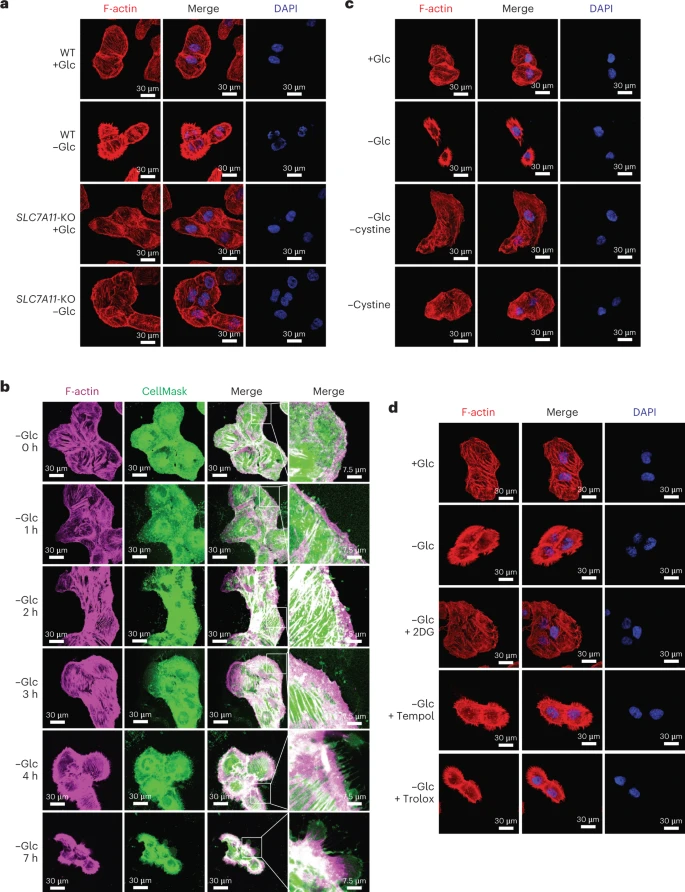
图 5: WRC和Rac调控disulfidptosis
CRISPR-Cas9筛选发现,WAVE调节复合体的部分组分在disulfidptosis中发挥作用,Rac激活状态下的细胞显著增加了disulfidptosis的发生。
细胞通过Rac-WRC途径调控的肌动蛋白的聚合和假足形成对维持细胞骨架稳定性尤为重要。
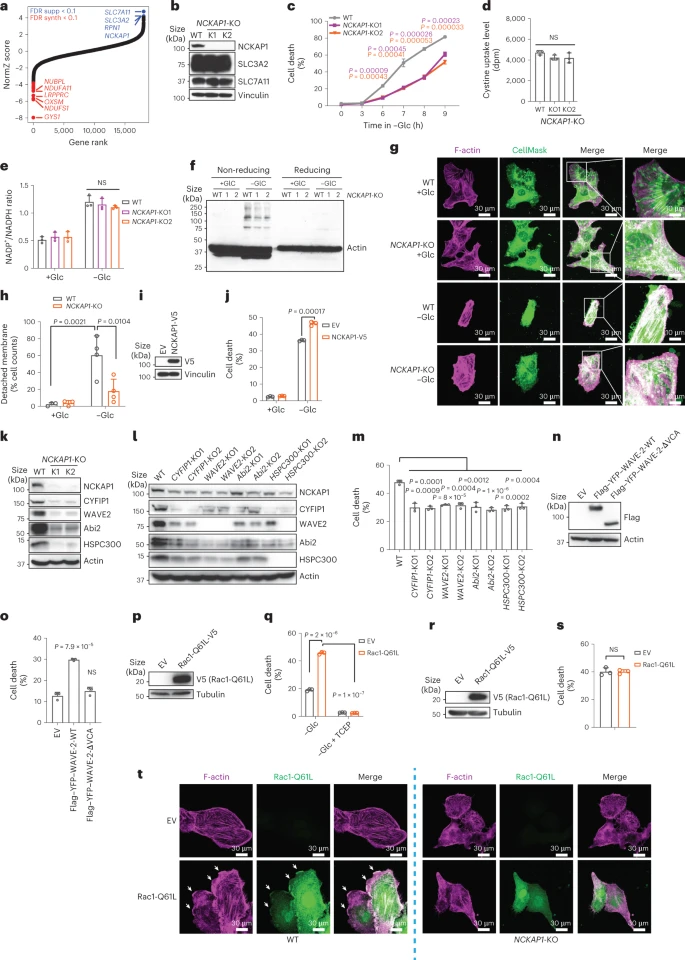
图 6: GLUT抑制剂在SLC7A11高表达细胞中诱导disulfidptosis
GLUT抑制剂BAY-876和KL-11743能显著降低葡萄糖摄取,增加NADP+/NADPH比率和促进disulfidptosis。
这一发现说明GLUT抑制剂可以作为治疗SLC7A11高表达肿瘤的潜在药物。
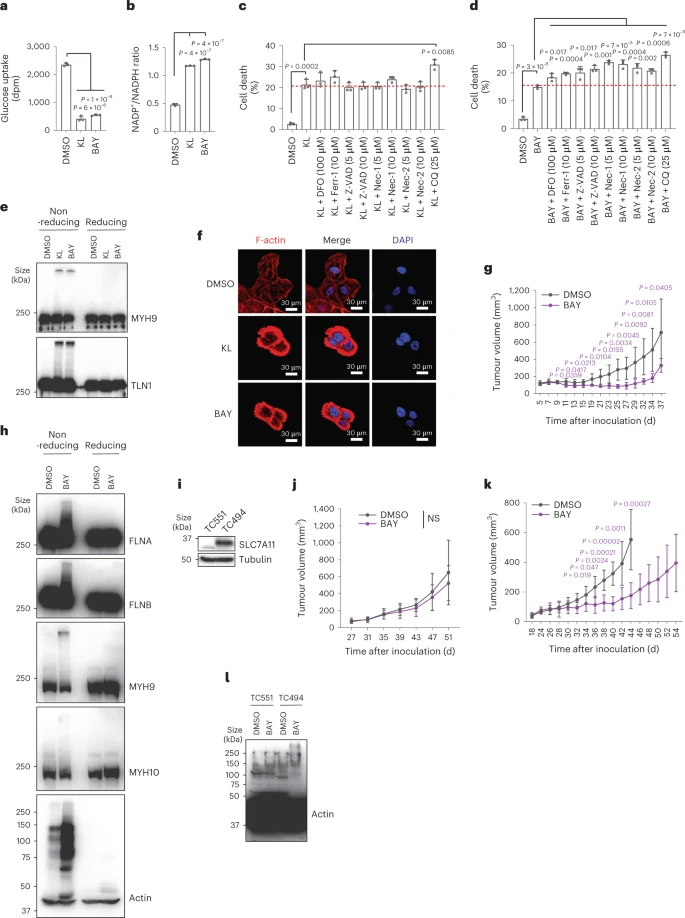
这些实验揭示了在SLC7A11高表达的癌细胞中,葡萄糖饥饿状态下细胞骨架对氧化应激的高度易损性,并证明了这一过程导致了特定的细胞死亡形式——disulfidptosis。进一步的研究可能会帮助我们利用这一发现来开发针对癌症治疗的靶向策略。
6主要结论
本研究揭示了硫化物应激对肌动蛋白骨架稳定性的影响,通过硫键相关细胞死亡途径导致细胞死亡。同时,研究提供了实验和动物模型证据支持该途径可作为新的抗癌目标,特别是针对SLC7A11高表达的肿瘤。
7讨论总结
硫键相关细胞死亡描述了一种由于内部二硫分子异常积累导致的细胞死亡形式。该研究扩展了我们对细胞死亡机制的认识,并且提供了一种治疗SLC7A11高表达肿瘤的潜在策略。未来的研究将需要进一步探索除了肌动蛋白骨架外,可能参与硫键相关细胞死亡的其他途径。同时,对硫键相关细胞死亡的调控机制和在各种代谢压力下导致的NADPH耗尽的情境下展开更深入的理解。













